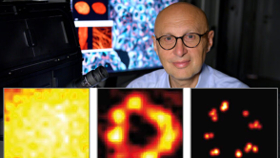
Was nie ein Mensch zuvor gesehen hat
(11.07.2023) Mit MINFLUX aus Stefan Hells Labor lassen sich Konformationsänderungen einzelner Proteine nanometergenau auf der Millisekunden-Skala verfolgen.
Haben Sie Proteinen schon einmal bei der Arbeit zugeschaut? Nein, nicht etwa photometrisch in einem enzymatischen Assay, sondern in echt? Weder ein herkömmliches noch ein konfokales Mikroskop wird dafür genügen. Denn aufgrund der Beugung von Licht hat das Auflösungsvermögen normaler Lichtmikroskope physikalisch vorgegebene Grenzen von 200 bis 300 Nanometern. Die Größe von Proteinen liegt jedoch im unteren Nanometerbereich. Das grün fluoreszierende Protein (GFP) mit seinen 238 Aminosäuren und 28 Kilodalton beispielsweise misst nur 4,2 Nanometer mal 2,4 Nanometer.
Liegen mehrere Moleküle darüber hinaus beisammen, verschwimmen ihre Konturen. Sie dann inmitten uninteressanter Moleküle sichtbar zu machen, ist der wesentliche Vorteil von Fluoreszenzmikroskopie. Doch erneut ist die Aussagekraft begrenzt: Auf kleinem Raum, etwa innerhalb des Zellkerns, erscheinen auch Fluorophor-markierte Moleküle nur als leuchtende Wolke. Diese verrät zwar, was das Lieblingsorganell eines Moleküls ist, doch ob es sich rege bewegt, mit anderen Zellkomponenten interagiert oder nur faul herumliegt, bleibt unbekannt.
Die Entwicklung der Stimulated Emission Depletion (STED)-Mikroskopie durch die Arbeitsgruppe des Göttinger Physikers Stefan Hell um das Jahr 2000 änderte das. STED läutete die Ära der superauflösenden Fluoreszenzmikroskopie ein, zu der auch das ein paar Jahre später beschriebene und unter den Bezeichnungen Photoactivated Localization Microscopy (PALM) beziehungsweise Stochastic Optical Reconstruction Microscopy (STORM) bekannte Verfahren zählen. Da STED und PALM/STORM mit ihrer Auflösung von 20 bis 30 Nanometern die sichtbare Detailtreue um den Faktor zehn verbesserten, wurden ihre Entwickler mit dem Chemienobelpreis 2014 gewürdigt.
Beiden Techniken liegt zugrunde, dass Fluoreszenzsignale gezielt an- und abgeschaltet werden können. PALM/STORM sammelt dafür die Signale einzelner Fluorophore und konstruiert daraus ein Mikroskopiebild. STED unterbindet hingegen das Leuchten fluoreszenzfähiger Moleküle abseits eines fokussierten Mittelpunkts, indem ein ringförmiger Laserstrahl um den Mittelpunkt herum intensives Licht einer energieärmeren Wellenlänge einstrahlt. Sowohl STED als auch PALM/STORM sind darauf angewiesen, möglichst viele Photonen von Fluorophoren einzusammeln. Währenddessen vergeht Zeit, in der sich Moleküle bewegen und Fluorophore irreversibel ausbleichen können.
Superauflösung 2.0
Seinen Trick mit dem ringförmigen „Donut“-Laserstrahl entwickelte Stefan Hell natürlich weiter und stellte mit seiner Arbeitsgruppe im Jahr 2017 schließlich Minimal Photon Fluxes (MINFLUX) vor (Science, 355(6325):606-12). Auch MINFLUX lokalisiert Fluorophor-markierte Moleküle. Erneut rastert ein „Donut“-Laser dafür eine flächige Probe ab, sucht diesmal aber nach möglichst schwachen Fluoreszenzsignalen. Aus den Fluoreszenzdaten erkennt das MINFLUX-System iterativ, in welcher Richtung und mit welcher Schrittgröße sich das Anregungsminimum des Lasers weiter an ein fluoreszierendes Molekül herantasten muss, bis es schließlich ein minimales Fluoreszenzsignal – im besten Fall das Hintergrundniveau – detektiert. Denn dann fällt das zentrale Anregungsminimum des „Donut“-Lasers punktgenau mit dem Fluorophor zusammen. Aus der bekannten Position des Lasers lässt sich auf die Position des Fluoreszenzmoleküls rückschließen.
Der Vorteil ist klar: Während PALM/STORM nach Signalmaxima sucht, schont MINFLUX Fluorophore. Photobleichung ist kein Thema mehr. Im Vergleich zu PALM/STORM reichen für die gleiche Lokalisationsgenauigkeit hundertmal weniger Photonen aus. Ist die Position eine Fluorophors bereits nanometergenau bekannt, kommt MINFLUX sogar mit 20 bis 40 Photonen aus, um jede weitere Positionsveränderung auf den Nanometer genau zu detektieren. Das macht ein Einzelmolekül-Tracking nicht nur hundertmal schneller als bisher, sondern verringert das Auflösungslimit nochmals um einen Faktor zehn auf die molekulare Skala von ein bis drei Nanometern.
Kein Ende in Sicht
Natürlich war die Gruppe von Stefan Hell, der als Direktor an den beiden Max-Planck-Instituten für multidisziplinäre Naturwissenschaften in Göttingen und für medizinische Forschung in Heidelberg tätig ist, auch seit 2017 nicht untätig. Ihre aktuelle MINFLUX-Variante verwendet anstelle des „Donut-Lasers“ drei orthogonale Strahlenpaare, die Proben entlang aller drei Raumrichtungen in immer feiner werdenden Schritten abtasten. Ein Blick unter ihre Motorhaube: Mithilfe von Phasen- und Amplitudenmodulatoren wird ein 640-Nanometer-Laserstrahl so geformt, dass ein Strahlenpaar mit einer definierten Phasendifferenz entsteht. Deren destruktive Interferenz erzeugt ein Intensitätsmuster mit einem nicht Donut-, sondern linienförmigen Minimum in der Brennebene. Zwei solcher Strahlenpaare decken die x- und die y-Richtung ab. Für 3D-Aufnahmen kommt noch ein Strahlenpaar in z-Richtung hinzu. Durch Änderung der Phasendifferenzen können alle Anregungsminima mit einer Genauigkeit im Ångström-Bereich verschoben werden.
Was macht linienförmige Anregungsminima gegenüber dem „Donut“-Laser überlegen? Die Genauigkeit, mit der MINFLUX eine Struktur lokalisieren kann, wird durch die Steilheit des Intensitätsübergangs an der Grenze von fluoreszierendem Molekül und Hintergrundrauschen bestimmt. Ist diese Grenze abrupt und dazu die Hintergrundintensität niedrig, ist der Übergang steil. Und eben das ist der Vorteil des aktuellen MINFLUX-Mikroskops: Seine linienförmigen Anregungsminima liefern von Haus aus eine höhere Steilheit im Vergleich zu Donut-basierten Systemen. Dadurch ist der nichtangeregte Mittelpunkt des Lasers präziser definiert und Fluorophore können schärfer unterschieden und lokalisiert werden.
Das Ganze funktioniert sogar, wenn die scannenden Laser einem beweglichen Fluoreszenzmolekül hinterherlaufen. Entsprechend eignet sich MINFLUX zur reinen Lokalisierung eines Moleküls ebenso wie zum Molekül-Tracking. Hell ergänzt: „Der Imaging-Modus verwendet aktivierbare Farbstoffe und liefert schärfere Bilder als PALM/STORM oder STED. Dafür können beim Molekül-Tracking nichtschaltbare Fluorophore verwendet werden, die mehr Photonen abgeben“.
Gamechanger
Den erneuten Auflösungsgewinn tut Stefan Hell indes lapidar ab: „Ja, unser interferometrisches MINFLUX bringt im Vergleich zum 2017er-Gerät nochmal eine etwa 30-prozentige Verbesserung“. Der wesentliche Punkt ihrer aktuellen Publikation bestünde aber darin, der Wissenschaftsgemeinde das Anwendungspotenzial von MINFLUX zu demonstrieren. Hell sagt: „Die Detailliertheit der Mikroskopiebilder ist einzigartig. Ein Gamechanger! Erstmalig lassen sich sogar Konformationsänderungen von Proteinen beobachten“.
Hells Worte schwingen vor Begeisterung. Die Wahl eines geeigneten Demo-Objekts schien beinahe Nebensache. „Lass uns das Verfahren auf irgendwas anwenden“, sagte er seinen Leuten in der Arbeitsgruppe. Am Ende fiel die Wahl auf das Motorprotein Kinesin-1, das für die Bewegung von Organellen, Vesikeln und anderen Zellbestandteilen entlang von Mikrotubuli im Zellinneren verantwortlich ist. Kinesin-1 liegt als Dimer vor. Jedes Monomer umfasst eine Kopfregion, die Mikrotubuli bindet und eine katalytische Domäne enthält, sowie einen langen Stiel und einen Schwanzteil, der mit der zu transportierenden Fracht interagiert. Durch Hydrolyse von ATP verändert sich die Konformation der Kopf- und Halsbereiche und das Motorprotein tätigt einen acht Nanometer langen Schritt.
Die Publikation der Hell-Gruppe erschien zeitgleich mit einem Artikel der Arbeitsgruppe von Jonas Ries vom EMBL in Heidelberg, die die Kinesin-1-Bewegung ebenfalls mit MINFLUX untersuchte (Science, 379(6636:1010-5). „Das hat sich rein zufällig so ergeben, obwohl beide Gruppen in Heidelberg ansässig sind“, erinnert sich Hell. „Wir haben die thematische Überlappung erst gemerkt, als die Arbeit schon weit fortgeschritten war und uns entschieden, die Manuskripte am selben Tag beim selben Journal einzureichen. Die konkreten Inhalte haben wir gegenseitig nicht voneinander gekannt, aber wir haben ein gutes Verhältnis, auch wenn es keine Kooperation war.“ Während Hells Gruppe am Heidelberger MPI die Bewegung des Motorproteins in vitro mithilfe ihres interferometrischen MINFLUX und etablierten Fluoreszenzfarbstoffen untersuchte, arbeitete Ries‘ Gruppe am EMBL mit Lebendzellen, dem „Donut“-Laser-MINFLUX und einem weiterentwickelten Fluorophor. Die Ergebnisse beider Projekte bestätigen sich gegenseitig.
Neue Maßstäbe
Was genau umfasste Hells Projekt? Die Experimentatoren um die Erstautoren Jan Otto Wolff und Lukas Scheiderer markierten unterschiedliche Aminosäurereste von Kinesin-1 per Maleimid-Kopplung mit dem rot emittierenden Fluoreszenzfarbstoff Atto647N. Da der Fluorophor über Cysteinreste bindet, von denen Kinesin-1 fast ein Dutzend besitzt, war es nötig, diese zu mutieren beziehungsweise künstliche Cysteinreste an ausgewählten Positionen einzubringen. Fluoreszenz-markiertes Kinesin-1 gaben die Heidelberger schließlich zu Mikrotubuli, die sie auf Deckgläschen immobilisiert hatten. Wie erwartet bewegte sich Kinesin-1 in Gegenwart von ATP mit acht Nanometer langen Schritten vorwärts. Das war wenig überraschend.
Außergewöhnlich an den Experimenten der Heidelberger ist, dass MINFLUX erstmals Beobachtungen unter physiologischen ATP-Konzentrationen im Bereich von einem Millimolar ermöglichte. Denn bislang musste das Nucleotid stark verdünnt werden, um das Lauftempo von Motorproteinen durch Energiemangel zu drosseln und überhaupt etwas beobachten zu können. Da MINFLUX aber so wenige Photonen benötigt, kann es auch schnelle Bewegungen aufzeichnen. Damit liegt der neue Rekord räumlich-zeitlicher Auflösung bei 1,7 Nanometern pro Millisekunde. „Das ist 50- bis100-mal schneller, als es bisher möglich war“, jubelt Hell.
Abgesehen von Geschwindigkeitsrekorden beantworteten die Experimente auch die seit langem offene Frage, wann das Motorprotein ATP bindet und hydrolysiert. In seinem 1HB-Zustand ist Kinesin-1 nur mit seinem führenden Kopf an Mikrotubuli gebunden. Im 2HB-Zustand wechselwirken die Köpfe beider Dimere mit ihren jeweiligen Mikrotubuli-Bindungsstellen. Mithilfe eines langsam hydrolysierbaren ATP-Analogs (ATPγS) erreichte Hells Arbeitsgruppe einen 36-fachen Zeitlupeneffekt und erkannte: ATP bindet im 1HB-Zustand, wenn sich der ungebundene Kopf zwischen der vorherigen und der nächsten Bindungsstelle befindet. Die ATP-Hydrolyse findet erst statt, nachdem sich der ungebundene Kopf zu seiner nächsten Bindungsstelle bewegt hat.
Kommerzielle MINFLUX-Geräte sind neben dem EMBL auch an Forschungsinstituten in Jena, Shanghai und Peking im Einsatz. In den US-amerikanischen National Institutes of Health (NIH) stehen sogar zwei Geräte. „Die Publikationszahlen schnellen in die Höhe. MINFLUX ist eines der heißesten Mikroskopie-Verfahren derzeit“, erklärt Stefan Hell mit einem Augenzwinkern.
Andrea Pitzschke
Wolff J. et al. (2023): MINFLUX dissects the unimpeded walking of kinesin-1. Science, 379(6636):1004-10.
Dieser Artikel (zusammen mit einem Interview mit dem Nobelpreisträger) erschien zuerst in Laborjournal 6/2023.
Bild: AG Hell/MPI-NAT (2)
Weitere Artikel zum Thema Mikroskopie
- Scharfe Bilder mit verbeulten Objektiven
Der Deutsche Zukunftspreis, der Preis des Bundespräsidenten für Technik und Innovation, ging im letzten Jahr an drei Forscher der Firma Zeiss für die Entwicklung eines Lattice-Lightsheet-Mikroskops. Aber diese Technologie ist doch gar nicht neu. Wofür also gab es den Preis?
- Auf starkem Expansionskurs
Die Idee der Expansionsmikroskopie (ExM) ist simpel: Statt sündhaft teure hochauflösende Mikroskope anzuschaffen, um die Beugungsgrenze zu umgehen, vergrößert man einfach die Probe. Die geringeren Kosten sind aber nicht der einzige Grund, warum die ExM immer mehr Anhänger findet.
- Superauflösende Mikroskopie für jeden
Von der superauflösenden Mikroskopie konnten viele Gruppen bisher nur träumen, weil die Geräte zu teuer sind und ihre Bedienung kompliziert ist. Mit der One-Nanometer-Expansionsmikroskopie könnte sich dies ändern.