Bernsteinsäure
aus dem Bioreaktor
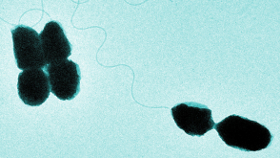
(21.03.2022) Das Meeresbakterium Vibrio natriegens ist genügsam und wächst flott. Metabolisch optimiert produziert es Succinat ökonomisch und ökologisch.
Bernsteinsäure oder Succinat lernt jeder Schüler irgendwann als Intermediat des Tricarbonsäure-Zyklus kennen. Der C4-Körper mit zwei endständigen Carboxylgruppen (Dicarbonsäure) ist aber auch in chemischen Synthesen gefragt – als Ausgangssubstanz für die Produktion von verschiedenen Verbindungen, die in Pharmazie, Kosmetik oder Lebensmitteltechnologie zum Einsatz kommen. Als Vorstufe von wertvollen Produkten wie Kunststoffen und Lösungsmitteln gehört Bernsteinsäure zu den zwölf wichtigsten Plattform-Chemikalien, die zukünftig ausschließlich biobasiert produziert werden könnten. Doch das ist Zukunftsmusik: Noch wird ein Großteil der Dicarbonsäure auf Basis von Rohöl, aus Butan oder Benzen, gewonnen.
Dabei gibt es bereits einige biotechnologisch nutzbare Mikroorganismen, die für die Produktion von Bernsteinsäure eingesetzt werden können. Dazu gehören sowohl Bakterien wie Escherichia coli und Corynebacterium glutamicum, aber auch Hefen wie Saccharomyces cerevisiae und Yarrowia lipolytica. Zusätzlich gibt es eine Reihe weniger gut erforschter Bakterien, die natürlicherweise große Mengen an Succinat ausscheiden wie beispielsweise Actinobacillus succinogenes und Vertreter der Gattungen Anaerobiospirillum, Mannheimia und Basfia, deren gemeinsames Epitheton „succiniciproducens“ bereits auf ihre Eigenschaft als Succinat-Produzenten hinweist. Damit eine biotechnologische Gewinnung von Succinat wirtschaftlich sinnvoll ist, muss das Produkt allerdings mit hoher Ausbeute und in hoher Konzentration gewonnen werden können. Außerdem sollten die Produzenten möglichst auf günstigen Medien wachsen.
Vielseitiges Meeresbakterium
Einen neuen Kandidaten ins Rennen schickt nun Bastian Blombach, Professor für Mikrobielle Biotechnologie an der TU München: das Meeresbakterium Vibrio natriegens, das durch extrem schnelles Wachstum und hohe Substrat-Aufnahmeraten für die biotechnologische Nutzung besonders attraktiv ist. „Mit einer maximalen Verdopplungszeit von nur ca. neun Minuten ist V. natriegens das am schnellsten wachsende, nicht-pathogene Bakterium. Außerdem ist die Genomsequenz bekannt, und es steht eine Vielzahl an molekularbiologischen Werkzeugen für die Manipulation zur Verfügung“, fasst Blombach die Vorzüge des Gamma-Proteobakteriums zusammen.
Ein weiterer Vorteil ist, dass V. natriegens auf Minimalmedium mit Glucose als einziger Kohlenstoff- und Energiequelle wachsen kann – und das sowohl in Anwesenheit von Sauerstoff als auch unter Sauerstoff-Ausschluss. Selbst Zellen, die sich unter anaeroben Bedingungen nicht mehr vermehren, vergären Glucose noch immer mit hoher Umsatzrate zu den Produkten Acetat, Formiat, Ethanol, Succinat und Lactat. Zusätzlich scheiden sie große Mengen an Alanin aus, was sich ebenfalls biotechnologisch nutzen lässt, wie Blombach und sein Team bereits 2017 in einer Veröffentlichung gezeigt haben (Appl Environ Microbiol, 83(22):e01614-17). Nun haben Blombach, Postdoktorand Felix Thoma und Kollegen einen Produktionsstamm vorgestellt, der für die Succinat-Gewinnung maßgeschneidert ist. Dafür wurden im ersten Schritt die Prozessbedingungen verbessert und anschließend konkurrierende Stoffwechselwege ausgeschaltet sowie auffüllende (anaplerotische) Reaktionen verstärkt.
Umgekehrter Tricarbonsäure-Zyklus
V. natriegens kann Bernsteinsäure sowohl unter aeroben als auch unter anaeroben Bedingungen herstellen. In der Glycolyse entsteht Pyruvat, das über das Zwischenprodukt Acetyl-CoA in den Tricarbonsäure-Zyklus einfließt, aber auch den Ausgangspunkt für die Produktion von Säuren und Alkoholen darstellt. Unter aeroben Bedingungen läuft der „klassische“ oxidative Tricarbonsäure-Zyklus ab, unter anaeroben Bedingungen kehren sich die Reaktionen des Stoffwechselwegs zum reduktiven Tricarbonsäure-Zyklus um. Dieser Weg endet bei Succinat, das ins Medium ausgeschieden wird.
Im ersten Schritt haben sich Blombach und sein Team angeschaut, wie viel Succinat aus zugesetzter Glucose über die verschiedenen Stoffwechselwege gewonnen werden kann. Als Ausgang für ihre Optimierung verwendeten sie einen Wildtyp-Stamm, den sie unter anaeroben Bedingungen in Minimalmedium mit Glucose als einziger Energie- und Kohlenstoffquelle anzogen. Unter diesen Bedingungen wurde keine Energie mehr für die Vermehrung verbraucht. Dafür produzierte der Stamm 0,15 Mol Succinat pro Mol Glucose.
Durch zwei Eingriffe in den Produktionsprozess konnte bereits eine deutliche Steigerung der Ausbeute erreicht werden: Zum einen wurden zum Animpfen nicht wie sonst üblich Übernacht-Kulturen in der stationären Wachstumsphase verwendet, sondern solche, die gerade exponentiell wuchsen. Zum anderen wurde dem Medium Kaliumhydrogencarbonat (KHCO3) zugesetzt, um zu gewährleisten, dass genug CO2 für die Carboxylierung von Phosphoenolpyruvat und Pyruvat zur Verfügung steht. Diese anaplerotischen Reaktionen erzeugen Oxalacetat; wie Succinat eine Dicarbonsäure und Intermediat des Tricarbonsäure-Zyklus, den es sozusagen wieder auffüllt, nachdem ihm kontinuierlich Succinat entzogen wird. Die Ausbeute stieg dadurch auf 0,38 Mol Succinat pro Mol Glucose.
Genetisch optimiert
Im nächsten Schritt ging es an die genetische Optimierung des Produktionsstamms. Durch die Inaktivierung von einzelnen Genen wurden verschiedene Stoffwechselwege, die in der Zelle mit der Succinat-Produktion konkurrieren, ausgeschaltet oder zumindest stark geschwächt. Dazu zählten insbesondere die Synthesewege, die aus Pyruvat Lactat, Acetat, Formiat und Ethanol herstellen. Zusätzlich wurde das Gen für eine potenzielle Alanin-Dehydrogenase ausgeschaltet, in der Hoffnung, auf diese Weise die Produktion von Alanin, das in großer Menge ausgeschieden wurde, zu reduzieren. Daraufhin wurde zwar tatsächlich weniger Alanin gebildet, aber die Succinat-Ausbeute stieg kaum an. Am Ende dieser Schritte lag die Succinat-Ausbeute bereits bei 1,01 Mol pro Mol Glucose.
Die genannten genetischen Änderungen zielten darauf ab, die Verfügbarkeit von Pyruvat in der Zelle zu erhöhen. Allerdings fehlt V. natriegens eine Pyruvat-Carboxylase, die für die Umwandlung von Pyruvat zu Oxalacetat notwendig ist. Durch die Einführung des Gens für die Pyruvat-Carboxylase aus C. glutamicum stärkten die Straubinger diesen anaplerotischen Reaktionsweg und verbesserten dadurch die Succinat-Ausbeute auf 1,46 Mol pro Mol Glucose – ein Wert, der bereits 85 % des theoretischen Maximums entspricht.
Trotz der Inaktivierung von Genen für die Acetat-Produktion wurden weiterhin 12 Prozent der Glucose in Acetat umgesetzt, das damit das wichtigste Nebenprodukt darstellt. Ein erneuter Versuch, die Acetat-Produktion zu reduzieren, führte dazu, dass der Stamm nicht mehr auf Minimalmedium wachsen konnte und wurde deshalb nicht weiter verfolgt.
Produktiv und anspruchslos
Durch die Optimierungsschritte konnte die Succinat-Ausbeute bereits 10-fach gesteigert werden. In den Kultivierungsansätzen war die eingesetzte Glucose jedoch nach 2-3 Stunden umgesetzt, sodass die Gesamtausbeute natürlicherweise limitiert war. Die Biotechnologen stiegen deshalb auf einen Bioreaktor im Labormaßstab um, in dem Kaliumhydrogencarbonat zugefüttert werden konnte. Außerdem ließ sich der pH-Wert regulieren, der sonst durch die Succinat-Produktion kontinuierlich absinken würde. Auf diese Weise konnte die Succinat-Produktion über mehrere Stunden fortgesetzt werden. Zwar lag die Ausbeute unter diesen Bedingungen bei nur noch 1,14 Mol Succinat pro Mol Glucose, doch in 7 Stunden wurden insgesamt 60,4 g pro Liter Succinat gebildet. Umgerechnet auf eine Stunde sind dies 8,6 g pro Liter und damit deutlich mehr als die 2,5 g pro Liter, pro Stunde, die als Produktivitätsuntergrenze für eine wirtschaftliche Succinat-Gewinnung gelten.
„Hinsichtlich der Succinat-Ausbeute sind wir im Kulturkolben schon ganz oben dabei“, freut sich Thoma. „Auch im Bioreaktor liegen wir schon bei über 90 % der Ausbeute von M. succiniciproducens.“ Und Blombach fügt hinzu: „Der große Vorteil von V. natriegens ist sein prototrophes Wachstum. Im Gegensatz zu M. succiniciproducens wächst er auf kostengünstigen Minimalmedien und benötigt keine Supplementation von Aminosäuren, Vitaminen oder anderen komplexen Medienbestandteilen.“ Trotz dieser schon sehr guten Ergebnisse möchten die Straubinger den Produktionsstamm noch weiter optimieren: „Wir möchten einen Prozess etablieren, bei dem Biomassebildung und Produktion in einem Reaktor ablaufen. Außerdem wäre es toll, wenn wir unseren Produktionsstamm so anpassen könnten, dass er statt Glucose Lignocellulose-Hydrolysate als Kohlenstoff- und Energiequelle verwenden kann.“ Sollte dies gelingen, könnte V. natriegens Holzabfälle in Succinat umwandeln. Nachhaltiger geht es eigentlich nicht mehr!
Larissa Tetsch
Thoma F. et al. (2021): Metabolic engineering of Vibrio natriegens for anaerobic succinate production. Microb Biotechnol, DOI: 10.1111/1751-7915.13983
Bild: Mikrobielle Biotechnologie/TUM
Weitere Journal Clubs aus dem Laborjournal-Archiv
- Ausgebremste Konkurrenten
Jedes Spermium besitzt seine ganz eigene Mischung an Genen. Welches von ihnen seinen Erbgut-Cocktail an die nächste Generation weitergeben kann, hängt weitgehend vom Zufall ab. Außer manche tragen ein egoistisches genetisches Element ...
- Wirkung im Widerspruch
Dass ein Wirkstoff einen Rezeptor gleichzeitig hemmt und verstärkt, klingt erst einmal paradox. Doch genau das hat ein Team von der Ruhr-Universität Bochum kürzlich dokumentiert und den Mechanismus hinter dem Paradoxon entschlüsselt.
- Verjüngungskur für Taufliegen
Ringförmige RNA-Moleküle sind lange bekannt – was sie machen, weiß keiner so genau. In Taufliegen wurde nun erstmals ein Zusammenhang mit dem Alterungsprozess gezeigt.