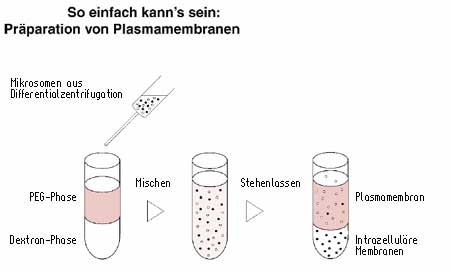
Isolierung von Plasmamembranen
Grüne wissen's manchmal besser
Hubert Rehm
Nichts ist perfekt, an allem gibt es was zu kritteln, selbst am Experimentator. Sabine Luthje von der Universität Hamburg stellte fest, daß selbst in der 4. Auflage des
Experimentator Proteinbiochemie/Proteomics für die Isolierung der Plasmamembran noch die Sucrosegradientenzentrifugation empfohlen wird. Dies sei seit Mitte der 80er Jahre obsolet. Man verwende heute ein wäßriges Zwei-Phasensystem aus Polyethyleneglykoll (PEG) und Dextran.
Frau Luthje hat recht. Ihr sei Dank. Schande über mich.
Rot weiß nix von Grün
Es richtete mein Ego wieder etwas auf, als ich entdeckte, daß ich nicht der einzige war, dem das Zweiphasensystem entgangen ist: Selbst im 21. Jahrhundert werden Plasmamembranen noch mit Sucrosegradienten isoliert.
Das liegt daran, daß sich die Zweiphasen-Methode zuerst und vor allem unter Botanikern, den Grünen, verbreitete. Christer Larsson, von dem die Methode stammt, isolierte damit Plasmamembranen aus Spinat. Larsson hat die Methode u.a. in
Modern Methods of Plant Analysis New Ser. Vol. 1 (1985), Springer Verlag, Seite 85-104 veröffentlicht (auch diese Literaturstelle verdanke ich Frau Luthje).
Vielen roten Biochemikern scheint dieser Trend zur Zweiphasen-Methode entgangen zu sein. Sie sind es, die nach wie vor zur Zuckertüte greifen, wenn sie Membranen isolieren wollen. Grüne und rote Biochemiker scheinen sich und ihre Werke zu ignorieren.
Dabei lassen sich mit der Zweiphasenmethode auch tierische Plasmamembranen isolieren. So aus Rattenleber (Navarro et al., Faseb J. 1998, 12: 1665-1673 oder Legare et al. AJP 2001, 280: E193-E196).
Um die roten Gemüter für die grünen Phasen empfänglich zu machen, werde ich - psychologischer Trick - erst mal die alte Gradientenmethode runtermachen.
Sucrosegradienten haben ja, sieht man von der ihnen innewohnenden Süßigkeit ab, einige Nachteile: Das Zeug ist klebrig und wird bei längerem Stehenlassen gerne von Pilzen befallen. Des weiteren erfordert das Gießen Konzentration und handwerkliches Geschick. Das Schlimmste aber ist: Sucrosegradienten trennen nach Dichte und Größe, Parameter, die breit über die Membranvesikel verteilt sind: Plasmamembranen unterscheiden sich in Größe und Dichte nur graduell von z.B. mitochondrialen Membranen. Die Plasmamembranen, die Ihnen der Sucrosegradient liefert, sind daher recht schmutzig. Bei Membranen aus Pflanzen schwimmen beispielsweise zwischen den Plasmamembranen noch Fragmente von Chloroplasten. Es ist auch nie klar, was Sie mit einem Sucrosegradienten erhalten: Versiegelte Vesikel? Undichte Vesikel? Außenteil nach außen oder Außenteil nach innen gewendet? In der Regel wohl eine Mischung aus allem, ein Membransalat.Die Experten für Salat haben dieses Problem gelöst.
Larssons Zweiphasen-Methode nutzt die Oberflächeneigenschaften der Membranen. Sie erhalten also Vesikel mit einheitlichen Oberflächen-Eigenschaften und daher Vesikel mit einheitlicher Ausrichtung: Entweder nur Outsideout-Vesikel oder nur Insideout-Vesikel. Vesikel aus Pflanzen sind Outsideout und meistens dicht.
Wie alle Methoden-Entwickler lobt Larsson seine Methode in den Himmel: Die Präparationen seien rein, schnell gemacht und ließen sich in großen Mengen herstellen. Schauen wir uns die Sache an.
Die Plasmamembran liebt PEG
Wenn Sie Dextran und PEG mischen, entstehen bei bestimmten Konzentrationsverhältnissen zwei Phasen: Eine PEG-reiche obere und eine dextranreiche untere. Der Hauptbestandteil beider Phasen ist Wasser bzw. ein entsprechender Puffer. Zur Isolierung von Plasmamembranen stellen Sie, z.B. in einem Falcontube, solch ein Zweiphasensystem her, geben ihre Membranpräparation dazu, schütteln und lassen das Tube dann eine Weile stehen oder zentrifugieren ab (3 Minuten bei 1500 g). Die beiden Phasen bilden sich aufs Neue. In der Oberen, der PEG-reichen Phase, schwimmen die Plasmamembranen, in der Unteren, der dextranreichen Phase, die intrazellulären Membranen aus Mitochondrien, Golgi-Apparat und endoplasmatischem Retikulum.
Ist das nicht wunderbar?
Leider nicht. Denn die Zweiphasentrennung hat einige Mucken. Die Trennung hängt ab von der Polymerkonzentration und der Salzkonzentration und -zusammensetzung. Des weiteren reicht ein einziger Trennungsschritt nicht aus. Sie müssen die Phasentrennung wiederholen, bei einer präparativen Reinigung mindestens zweimal.
Wichtig ist nicht nur von der Konzentration der Polymere, sondern auch der Batch des verwendeten Dextrans bzw. PEG. Und natürlich funktioniert das nicht mit jedem x-belieben Dextran oder PEG, es muß Dextran T 500 sein und PEG 3350 (hieß früher PEG 4000). Zudem müssen Sie für jede Membranpräparation die optimale Zusammensetzung ermitteln und danach noch mit der Salz-Konzentration herumspielen, denn auch die beeinflußt die Trennung.
Die Liebe der Ionen
Es ist so: Geben Sie Salz zu dem Zweiphasen-System, so verteilen sich die Ionen unterschiedlich. Bei Kaliumphosphat beispielsweise hat HPO
42--Ion eine höhere Affinität zur unteren Phase als K
+. Es entsteht eine elektrostatische Potentialdifferenz zwischen den Phasen, die obere Phase positiv. Ähnliches gilt für KCl und NaCl.
Die Potentialdifferenz beeinflußt das Verhalten der Membranen. So nimmt bei einem 5,7 % Dextran/5,7 % PEG-System der Anteil mitochondrialer Membranvesikel in der oberen Phase mit zunehmender Konzentration von KCl ab: Von etwa 50 % bei 0 mM KCl auf unter 10 % bei 5 mM KCl. Warum das so ist, ist, wie so vieles im Leben, unklar.
und der Membranen
Im allgemeinen gilt: Die Plasmamembranen stören sich nur in geringem Maße an den Konzentrationen von Polymer und Chlorid, sie bleiben in der oberen Phase. Beispiel: Bei 5 % Dextran/5 % PEG bleiben die Plasmamembranen 100-%ig oben, bei 7 % Dextran und PEG noch zu 90 %. Mit zunehmender Konzentration von Polymer verschwinden die intrazellulären Membranen in die untere Phase. Daher nimmt die Reinheit der Plasmamembranen zu. Intrazelluläre Membranen reagieren sehr empfindlich auf die Konzentration der Polymere. Unterschiede von einem halben Prozent haben riesige Auswirkungen.
Die größte Affinität für die dextranreiche untere Phase haben mitochondriale Membranen, gefolgt von Membranen des endoplasmatischen Reticulums und des Golgi-Apparates.
Die Phasentrennung ist Temperatur-sensitiv. Sie führen sie am besten im Kühlraum aus.
Da die Plasmamembranen als versiegelte Vesikel vorliegen, enthalten sie Cytoplasma und damit cytoplasmatische Proteine wie LDH. Die werden Sie los, indem sie die Membranvesikel aufbrechen und waschen, z.B. durch Resuspension in hypotonischem Medium. Waschen empfiehlt sich sowieso, denn Sie müssen das PEG loswerden, in dem die Vesikel nach der Reinigung schwimmen.
Der Mühen Lohn
Sie erhalten Plasmamembranen, deren Reinheit bei 99 % und darüber liegen soll. Die Vesikel sind von einheitlicher Dichte, geben z.B. nur eine Bande in Percoll- oder Sucrosegradienten. Die Ausbeute einer Drei-Schritt-Reinigung liegt bei 60-70 %. Apropos Reinheit: Die Reinheit von Enzymen bestimmt der Quotient "Aktivität durch Proteinmasse". Ähnliches gilt für die Reinheit von Membranen: Man bestimmt die Aktivität eines Enzyms, das spezifisch für den Membrantyp ist, eines Markerenzyms und bezieht die Aktivität auf die Proteinmasse der Membranen. Larsson verwendet Cytochrom c-Oxidase für mitochondriale Membranen, Antimycin A-resistente NADH-Cytochrom c-Reduktase für Membranen des endoplasmatischen Reticulums und IDPase für Golgimembranen. Als Marker für Plasmamembranen diente Larsson lichtreduzierbares Cytochrom, was hauptsächlich in Pflanzen und Pilzen vorkommt. Leider ist lichtreduzierbares Cytochrom nicht spezifisch für Plasmamembranen, es kommt in ähnlicher Menge im endoplasmatischen Reticulum vor. Besser wäre es wohl, die Plasmamembranen über die Bindung von Lektinen zu bestimmen, denn Plasmamembranen besitzen als einziger Membrantyp extrazelluläre Zuckerketten.
Rote Marker
Für tierische Zellmembranen existieren eine Reihe von Markern: Die berühmte Na
+/K
+-ATPase, 5' Nukleotidase, adrenalinsensitive Adenylatzyklase, Lektinbindung (Sie könnten die Vesikel sogar an einer Lektinsäule reinigen) und bei speziellen Geweben auch spezielle Marker. Im Muskel z.B. eignet sich die a-Bungarotoxinbindung (Acetylcholin-Rezeptor). Ein Problem hat auch der rote Biochemiker: Die Spezifität. Da die Proteine der Plasmamembran im Zellinneren hergestellt und in die Membran transportiert werden, tauchen sie immer auch auf intrazellulären Membranen auf. Dort jedoch auf der falschen Seite, d.h. die Zuckerketten glykosilierter Plasmamembranproteine schauen ins Vesikelinnere. Bei geschlossenen Vesikeln werden diese Marker daher nicht erfaßt.
Spannender als schon publizierte Methoden nachzukochen ist es, eigene zu erfinden. Uemura und Yoshida behaupten in Plant Physiol. (1983) 13, 586-591, dass intrazelluläre Membranen mit 10 mM ZnCl
2 aggregieren, Plasmamembranen dagegen nicht. Könnte dies die Grundlage einer schnellen Plasmamembranreinigung geben?
Letzte Änderungen: 08.04.2005