Epithel, öffne dich!
Juliet Merz
(12.10.2021) MÜNSTER: Epithelzellen sind Meister darin, die Kontaktstellen zu ihren Nachbarn abzudichten. Während der Entwicklung einer Drosophila-Eizelle gibt es jedoch einen Zeitpunkt, zu dem die Zellzwischenräume geöffnet werden – und der damit wichtige Einblicke in die Bildung von Epithelgeweben gibt.
Epithelzellen kleiden unseren Körper sowie unsere Organe aus und stehen dabei vor einem ständigen Dilemma: Auf der einen Seite sollen sie den Organismus vor schädlichen Stoffen und Krankheitserregern schützen, auf der anderen Seite sollen sie nützliche Moleküle und Helfer (etwa Immunzellen) durchwinken. Die Schutzfunktion erfüllen Epithelzellen, indem sie eng beieinander sitzend eine dichte Zellschicht bilden und die Zellzwischenräume mit Adhäsionsproteinen verkleben. Dadurch verlieren sie den Kontakt zu ihren Nachbarn nicht, und es gibt kein Durchkommen – fast. Denn wie ein Forschungsteam um den Entwicklungsbiologen Stefan Luschnig von der Universität Münster kürzlich zeigte, können Epithelzellen während der Entwicklung von Drosophila-Eiern ihre Zellzwischenräume an ganz spezifischen Stellen für den Stofftransport vorübergehend öffnen (Dev. Cell 56: 1–17).
Zelluläre Passierscheine
Epithelzellen können je nach Situation und Größe der Fracht zwei Transportrouten anbieten. Ein Weg führt direkt durch die Epithelzelle hindurch (transzellulär). Dadurch läuft die Aufnahme sicher ab, denn die Lieferung wird geprüft, und die Epithelbarriere bleibt weiterhin intakt. Der Nachteil: Transzelluläre Transporte sind kosten- und zeitintensiv. Schneller und günstiger geht’s mit der parazellulären Route. Dabei öffnet die Epithelbarriere die Durchgänge zwischen den Zellen, und Stoffe oder andere Zellen können einströmen. Sind die Tore allerdings erst einmal geöffnet, können auch ungeladene Gäste oder schädliche Stoffe passieren.
Die Ei-Follikel von Drosophila-Fliegen müssen während der Oogenese dieses Risiko eingehen. Sie haben aus Zeitgründen keine andere Wahl, wie Entwicklungsbiologe Luschnig erklärt: „Drosophila-Weibchen können täglich bis zu hundert Eier legen, sie müssen also sehr schnell befruchtungsfähige Eizellen produzieren.“
Luschnig leitet an der Universität Münster eine Arbeitsgruppe, die sich mit der Frage beschäftigt, wie sich Epithelgewebe ausbilden. Im Rahmen dieses Projektes nahmen er und seine Doktorandin Jone Isasti-Sanchez die Fliegen-Oogenese genauer unter die Lupe. Denn die Drosophila-Follikel sind ein ideales Studienobjekt, um die Bildung von Epithelbarrieren zu untersuchen. Der Grund: Zu einer bestimmten Zeit in ihrer Entwicklung öffnen sie die Zellkontakte selbstständig. „Das befruchtungsfertige Fliegen-Ei besteht zu einem Großteil aus Dotter, dessen Bestandteile aus der umliegenden Hämolymphe in das Ei-Follikel eingeschleust werden müssen“, so Luschnig, der sich schon zu seiner Doktorandenzeit mit der Frühentwicklung von Drosophila beschäftigte. Das Ei-Follikel besteht aus einem Follikel-Epithel aus somatischen Zellen, das eine Zyste aus Keimbahnzellen umhüllt. Die im Inneren des Follikels liegenden 16 Keimbahnzellen gehen aus einer Keimbahnstammzelle hervor. Es bleiben eine Oozyte und 15 sogenannte Nährzellen, welche die Oozyte mit Proteinen und RNAs versorgen.
Das Fliegen-Ei braucht zusätzlich eine große Menge an Dotter-Proteinen. Diese werden nur teilweise vom Follikel-Epithel selbst produziert, hauptsächlich aber vom Fettkörper der Fliege, dem Äquivalent zur menschlichen Leber und zum Fettgewebe. Die Dotter-Proteine müssen also von der Hämolymphe ins Innere des Follikels gelangen. „Während der Oogenese gibt es einen ganz spezifischen Zeitrahmen, in dem die Dotter-Proteine das Follikel fluten“, beschreibt Luschnig den circa 16 Stunden dauernden Öffnungsprozess (englisch „Patency“). Weil die Masse an Dotter-Proteinen so groß ist und die Oogenese schnell ablaufen muss, bleibt den Ei-Follikeln keine andere Wahl, als die parazelluläre Route zu öffnen. „Das Follikel-Epithel nimmt zwar vermutlich auch Dotter-Proteine über die transzelluläre Route – die Transzytose – auf und transportiert sie zur Oocyte, aber das reicht bei Weitem nicht aus“, weiß der Münsteraner Entwicklungsbiologe. Wir erinnern uns: Der transzelluläre Transport ist vergleichsweise langsam und dazu noch sehr energieaufwendig. Den Öffnungsprozess während der Insekten-Oogenese hatte schon 1972 ein kanadisches Forscher-Duo beschrieben und dabei beobachtet, dass die Dotter-Proteine vor allem zwischen den Epithelzellen wandern (J. Exp. Biol. 56: 201-14).
Aufgeschlossenes Dreiergespann
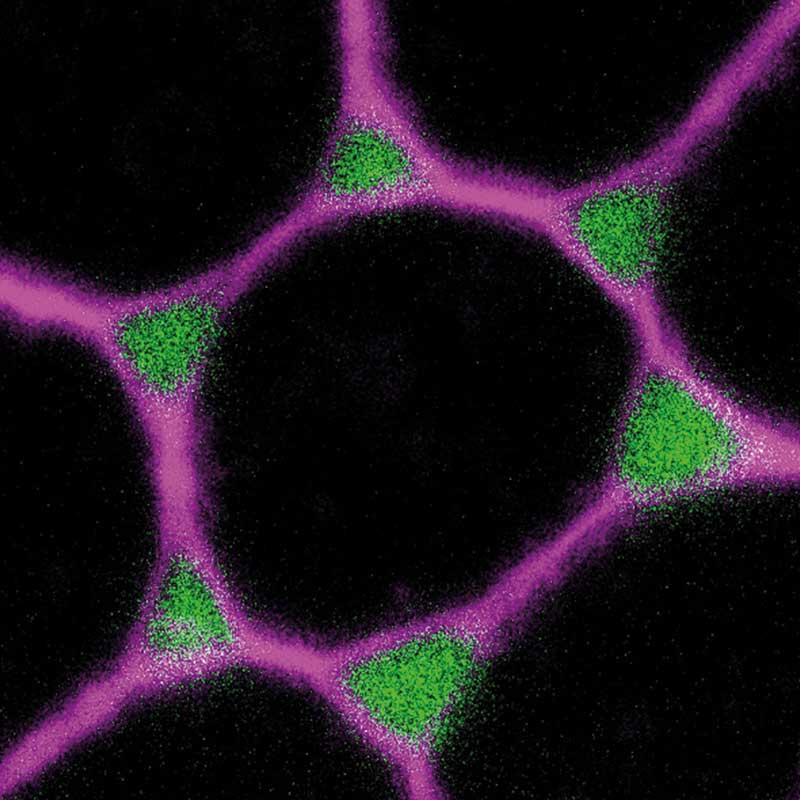
Erstautorin Isasti-Sanchez und Co. konnten nun zeigen, was während des Öffnungsprozesses auf molekularer Ebene abläuft. Luschnig: „Eine besondere Rolle spielen dabei die Kontaktstellen zwischen drei Zellen.“ Wenn man eine Epithelschicht von oben betrachtet, fallen zwei Kontaktstellen auf: Die Zelle berührt von allen Seiten je eine benachbarte Zelle, hier sind die bizellulären Kontaktpunkte (bizelluläre Junctions). Läuft man die Zellmembran imaginär entlang, endet die Kontaktstelle zur einen benachbarten Zelle irgendwann, und eine neue Nachbar-Zelle kommt ins Bild. Hier gibt es nun ein kleines Areal, in dem sich drei Zellen treffen – die trizellulären Junctions (siehe Bild oben).
Das Team fand heraus, dass sich zwischen diesen Drei-Zell-Kontakten vier unterschiedliche Adhäsionsproteine im Zuge des Öffnungsprozesses umorganisieren: N-Cadherin, E-Cadherin, Sidekick und Fasciclin2. Während E-Cadherin und Sidekick von der trizellulären Kontaktstelle zur bizellulären Seite hin abwandern, werden N-Cadherin und Fasciclin2 kurzerhand abgebaut. „Die Umlagerung beziehungsweise der Abbau der Adhäsionsproteine erfolgt in einer geordneten Weise. Dass es einen solchen Mechanismus gibt, der selektiv an Drei-Zell-Kontakten Adhäsionsproteine entfernt, war vorher nicht bekannt“, ordnet Luschnig ein und ergänzt: „Unsere Daten zeigen außerdem, dass für die Öffnung der trizellulären Junctions die Endozytose eine Schlüsselrolle einnimmt.“ Die Adhäsionsproteine werden demnach von den Epithelzellen über Endozytose ins Zellinnere aufgenommen und dann entweder abgebaut oder zu den bizellulären Junctions verfrachtet. „Die Adhäsionsproteine können zusätzlich möglicherweise lateral in der Membran von den trizellulären Junctions weg diffundieren – ob und in welchem Ausmaß das passiert, untersuchen wir derzeit genauer“, beschreibt der Entwicklungsbiologe eine aktuelle Forschungsfrage seiner Arbeitsgruppe.
Aber nicht nur die Adhäsionsproteine sind bei dem Öffnungsprozess während der Fliegen-Oogenese involviert. Auch das Zytoskelett verändert sich, wie die Münsteraner beobachten konnten. „Hier haben wir mit unserer Arbeitshypothese zuerst komplett daneben gelegen“, gibt Luschnig schmunzelnd zu. Durch das Wachstum der Oozyte und dem damit steigenden Druck im Inneren des Follikels hatte die Gruppe erst vermutet, das Zytoskelett der Follikelzellen würde an Spannung gewinnen – was möglicherweise als Signal für die Öffnung der trizellulären Junctions wirken könnte. Doch genau das Gegenteil ist der Fall: Die Spannung des Actomyosin-Zytoskeletts der Follikelzellen nimmt während der Oogenese ab. Die Entwicklungsbiologen hatten das Actomyosin-Zytoskelett dauerhaft mithilfe einer Kinase aktiviert, der Öffnungsprozess kam damit zum Erliegen. Daraus schlossen Luschnig und Co., dass das Zytoskelett während der Oogenese erschlaffen muss.
Geschickter Kompromiss
Dieser Öffnungsmechanismus ist die ideale Lösung für die Entwicklung der Fliegen-Eizelle: Das Follikel-Epithel öffnet die trizellulären Junctions, damit ausreichend Dotter-Proteine so schnell wie möglich einströmen können. Gleichzeitig bleiben die bizellulären Junctions fest verleimt, damit das Epithel nicht auseinanderfällt.
Gegen Ende der Vitellogenese, wenn das Follikel mit ausreichend Dotter ausgestattet ist, verschließen die Adhäsionsproteine die Drei-Zell-Kontakte wieder, und es bilden sich sogenannte Septate Junctions, die den dicht verschließenden Tight Junctions bei Wirbeltieren entsprechen. Das Epithel ist jetzt ausdifferenziert und öffnet die parazelluläre Route nicht mehr. Luschnig: „Es ist wichtig, dass der Öffnungsprozess bei der Oogenese Teil eines Entwicklungsprozesses ist. Das heißt, unsere Beobachtungen gelten nicht unbedingt in gleicher Weise für ein ausdifferenziertes Epithelgewebe, geben aber dennoch einen Einblick in die grundlegenden Mechanismen der Dynamik von Epithelbarrieren.“
Die Münsteraner Gruppe ist mit ihren Forschungen rund um die Öffnungsprozesse von Epithelzellen aber noch lange nicht am Ende. „Wir konnten mit unserer Studie einen ersten Einblick schaffen, wie die Prozesse ablaufen – vollständig verstehen wir sie aber noch nicht“, gibt Luschnig zu. Als Beispiel nennt er das Zusammenspiel zwischen der Erschlaffung des Zytoskeletts und der Umlagerung beziehungsweise dem Abbau der Adhäsionsproteine. „Welche molekularen oder physikalischen Trigger lösen die Öffnungsprozesse während der Oogenese aus?“, formuliert er eine der bleibenden Fragen.
Doch bevor die Gruppe erneut die Pipetten schwingt, muss sie zuerst einmal die Publikation in Developmental Cell nachfeiern. „Wegen Corona konnten wir nur im kleinen Kreis anstoßen, normalerweise machen wir das mit dem ganzen Institut“, sagt Luschnig und verrät, dass es kurz vor der Veröffentlichung des Papers sogar eine Art kleines Wettrennen gab. Dank der sich ausbreitenden Preprint-Kultur hatten die Münsteraner Entwicklungsbiologen per Zufall erfahren, dass eine Gruppe aus den USA ein Paper zur gleichen Thematik in der Pipeline hatte. Mittlerweile haben auch die US-amerikanischen Kollegen um Wu-Min Deng von der Tulane School of Medicine ihre Ergebnisse veröffentlicht (iScience 24: 102275). Luschnig erinnert sich ganz positiv: „Wir haben uns nach der Entdeckung des Preprints direkt mit den Kollegen in Verbindung gesetzt und offen kommuniziert, ohne jedoch direkt zu kollaborieren. Schlussendlich war es ein sehr positiver Austausch, obwohl – oder vielleicht gerade weil – ein gewisser Druck entsteht, die Ergebnisse zusammenzuschreiben.“