Stop-and-go auf der DNA
Juliet Merz
GÖTTINGEN: Während der Transkription legt die RNA-Polymerase II gerne mal eine Pause ein. Den Grund kennen Molekularbiologen zwar schon länger, wie genau die transkriptionelle Unterbrechung vonstattengeht, verstehen sie aber erst peu á peu..
Jeder braucht mal eine Pause – auch die RNA-Polymerase II während der Synthese von mRNA oder nicht-codierender RNA. Allerdings erholt sich der Enzymkomplex dabei nicht etwa von der anstrengenden Arbeit, er stoppt aus einem ganz anderen Grund.
Der Sinn hinter dem Polymerase-Stillstand ist naheliegend und schon lange kein Geheimnis mehr: Die Zelle verfügt damit über einen weiteren Schalter, um die Transkription zu regulieren. Doch wie die Pause initiiert wird, welchen Einfluss sie genau hat und welche Faktoren dabei eine entscheidende Rolle spielen, kommt erst allmählich ans Licht.
Patrick Cramer vom Max-Planck-Institut für biophysikalische Chemie in Göttingen ist schon seit Jahren an der Enthüllung rund um das transkriptionelle Stop-and-go beteiligt. Erst kürzlich konnte er gemeinsam mit der Biochemikerin Saskia Gressel und dem Mathematiker Björn Schwalb in einer Genom-weiten kinetischen Analyse zeigen, wie sich die Mobilität der Polymerase in humanen Zellen während einer Hitzeschock-Antwort verhält (Nat. Commun., doi: 10.1038/s41467-019-11536-8). Aber wie funktioniert das Stoppen des Enzymkomplexes überhaupt auf molekularer Ebene?
Blockade an den Genen
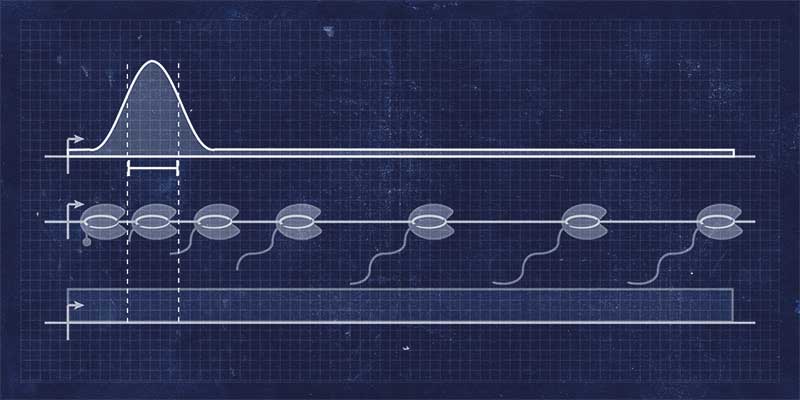
Bekanntlich bildet sich im ersten Schritt der Genexpression ein Vorinitiationskomplex an der Promotor-DNA. Der Komplex besteht aus der RNA-Polymerase II und zugehörigen Transkriptionsfaktoren. Anschließend beginnt die RNA-Synthese. Doch kurz nachdem die Polymerase über den Promotor gewandert ist, etwa 50 Basenpaare nach dem Transkriptionsstart, kommt sie zum Stehen. Maßgeblich an dem Prozess beteiligt sind die beiden Faktoren DSIF (5,6-Dichloro-1-beta-D-Ribofuranosyl-Benzimidazole (DRB) Sensitivity-Inducing Factor) und NELF (Negative Elongation Factor). Während DSIF rund um die DNA und RNA bindet, blockiert NELF die Mobilität der Polymerase, indem es an der gegenüberliegenden Seite des Enzyms andockt.
Doch bevor die Göttinger die durch die Pause induzierte Transkriptionsregulierung in humanen Zellen genauer untersuchen konnten, mussten sie Erfindergeist zeigen. Denn: „Die traditionelle Transkriptomik zählt die RNA-Moleküle in einer Zelle, die jedoch über Synthese und Abbau bestimmt sind“, meint Cramer. „Dadurch bekommt man keine Information über Transkription.“ Deshalb hatte Schwalb bereits 2016 zusammen mit Cramer und seinen ehemaligen Kollegen Margaux Michel und Julien Gagneur ein neues Verfahren namens TT-seq entwickelt, mit dem die Forscher einen präziseren Einblick in die RNA-Syntheseaktivität von Zellen erhalten (Science 352: 1225-8).
Die Grundidee von TT-seq basiert auf metabolischem Labelling. Dafür gaben die Forscher den Zellen ab einem bestimmten Zeitpunkt das Nukleotid-Analogon 4-Thiouridin ins Medium und reinigten es im Anschluss auf. Ein bisheriges Problem der Methode erklärt Schwalb: „Humane Gene sind sehr lang. Wenn wir nur einen kurzen Labelling-Impuls von etwa fünf Minuten wählen, wird das Label nur in einen Teilabschnitt der RNA eingebaut. In einer anschließenden Aufreinigung bekommen wir natürlich die komplette RNA und damit auch Moleküle, bei denen die Transkription beispielsweise schon vor einer halben Stunde gestartet ist.“ Um diesen Bias zu beseitigen, fügte die Gruppe einen zusätzlichen Schritt ins Protokoll ein: eine Fragmentierung. „So erhalten wir wirklich nur die RNA-Stücke, die in den vergangenen fünf Minuten transkribiert wurden“, meint Schwalb und ergänzt: „Die kinetische Auflösung dieser Methode ist extrem hoch.“
Die Regulierung der Gene durch die Pause der RNA-Polymerase II ist vor allem in zwei Situationen besonders wichtig: wenn sich die Zelle entwickelt oder unter Stress leidet. Cramer und Co. entschieden sich bei ihren Experimenten für einen Hitzeschock: Mit einem Anstieg von 37 auf 42 Grad Celsius versuchten sie die RNA-Polymerase II in der humanen hämatopoetischen Zell-Linie K562 aus der Pausen-Reserve zu locken. Mit Erfolg.
(Hitze)freie Fahrt
Die TT-seq-Daten zeigten zusammen mit Daten aus einem zweiten Ansatz, bei dem die Gruppe mittels einer Methode namens mNET-seq die Lokalisation der Polymerasen bestimmen kann, was sich auf Genomebene nach einem Hitzeschock in Zellen abspielt. Besonderes Augenmerk legte die Gruppe auf das Hitzeschock-Protein HSP70.
Während die Zellen bei angenehmen 37 Grad Celsius inkubierten, bewegte sich die RNA-Polymerase II stundenlang nicht von der Stelle, sondern wartete auf einer Sequenz unmittelbar nach dem Promotor des HSP70-Gens. Als die Forscher die Temperatur aufdrehten, begannen die Zellen auf den Stress zu reagieren. Sie verkürzten die Pause der Polymerase sehr deutlich. Außerdem schoss die Initiationsfrequenz in die Höhe, also die Anzahl von Polymerasen, die erfolgreich den DNA-Abschnitt transkribieren.
„Ist die Pause sehr lang, schränkt das ein, wie viele Polymerasen in das Gen ‚reinlaufen‘ können“, sagt Gressel. Und Cramer fasst zusammen: „Das hat ein großes Rätsel gelöst, weil lange nicht klar war, wie man mit der Pause überhaupt Gene regulieren kann. Wenn die Pause nur ein paar Minuten dauern würde, es aber beispielsweise eine Stunde dauert, ein menschliches Gen abzuschreiben, warum sollte es einen Unterschied machen, ob man zwei, vier oder sechs Minuten pausiert?“
Gressel und Schwalb hatten schon vor zwei Jahren gezeigt, dass die Pause ein Limit für die Initiation anderer Polymerasen setzt (eLife, doi: 10.7554/eLife.29736). Mit der aktuellen Studie ist es dem Team auch in vivo gelungen, eine natürliche Transkriptionsantwort zu studieren. Cramer: „Wir haben gesehen, dass die Zelle tatsächlich die Pausendauer verändert, um die Initiationsfrequenz nach oben setzen zu können, wenn sie Gene anschaltet.“
Die Pause scheint besonders für Gene wichtig zu sein, die sehr stark reguliert werden müssen – wie eben Gene für Entwicklung oder Überleben. Der Steady-State-Status der ruhenden Polymerase ermöglicht den Zellen, äußerst schnell zu reagieren, ohne erst noch den schwerfälligen Transkriptions-Apparat rekrutieren zu müssen. Quasi ein Polymerase-Vorrat direkt an besonders wichtigen Genen. „Die Pause findet grundsätzlich bei allen Genen statt“, klärt Gressel auf. „Sie kann Minuten oder sogar Stunden dauern. Das kommt darauf an, um welches Gen es sich handelt, welche Umwelteinflüsse auf die Zelle wirken oder in welcher Zellzyklusphase sie sich befindet.“
Die Forscher haben noch eine interessante Idee, wie es überhaupt zu der Pause gekommen sein könnte: „Wenn man Gene hat, die sehr hoch induzierbar sein müssen, sodass man starke Transkription kriegt, dann kann man am Kern-Promotor nichts mehr mutieren, denn der muss ohnehin optimal sein“, erklärt Cramer. „Wenn man aber zusätzlich regulieren möchte, was beim multizellulären Organismus sicher sehr wichtig ist, dann könnte man das über die Pausendauer tun – etwa durch Mutation im Pausenbereich abwärts des Promotors. Wir wissen nicht, ob das stimmt, aber es macht irgendwie Sinn.“
Doch was bringt die Polymerase eigentlich wieder zum Laufen? „Einer der wichtigsten Schalter der Transkriptionskontrolle der Zelle scheint CDK9 zu sein“, vermutet Cramer. CDK9 ist eine Kinase, die mit einem Cyclin zum positiven Transkriptions-Elongations-Faktor b (P-TEFb) gehört. Zusammen helfen sie der Polymerase, wieder sprichwörtlich in die Puschen zu kommen, indem sie zum einen die C-terminale Region der Polymerase phosphorylieren, aber auch negative Pausen-Faktoren gegen positive austauschen. Zur Erinnerung: NELF bindet an die Polymerase, um sie zu stoppen; P-TEFb phosphoryliert NELF und schafft den Faktor damit aus dem Weg.
Läuft etwas während dieses hoch regulierten Prozesses schief, kann das zu einer Vielzahl von Krankheiten führen, darunter zum Beispiel Krebs. „Die Zelle ist besonders sensitiv, was das Level von CDK9 angeht, weil dieser Schalter so wichtig ist“, weiß Gressel.
Obwohl die drei Göttinger schon viel in Erfahrung gebracht haben, schwirren ihnen noch einige ungelöste Fragen durch den Kopf: „Je mehr man weiß, desto mehr Fragen hat man“, schmunzelt Gressel. Besonders den Pausenverlauf während der Entwicklung findet das Team spannend. Aber auch, welche Rolle der Polymerase-Stopp bei Splicing-Prozessen haben könnte. Denn immerhin hat die Geschwindigkeit, mit der eine Polymerase über ein Gen gleitet, auch Einfluss darauf, welche Exons rausgeschmissen werden, wie Gressel erklärt. Cramer ergänzt noch einen Punkt: „Wie CDK9 letztlich zur Polymerase rekrutiert wird, ist auch noch nicht gut bekannt.“
Die perfekte Kombination
Die gute Zusammenarbeit zwischen Gressel und Schwalb war laut Cramer der Schlüssel für den Erfolg der Gruppe: „Wir sind hier nur weitergekommen durch die Kombination der beiden: Saskia Gressel ist die Experimentalistin, die Protokolle aufbaut, optimiert und Daten generiert. Und Björn Schwalb ist der Mathematiker und Informatiker, der ein theoretisches Modell erstellt hat, um aus den Daten die kinetischen Parameter zu extrahieren. Beides ist wichtig, aber der Trick ist, eine gemeinsame Sprache zu finden.“
Doch bis zum Ende dieses Jahres wird sich das Dreiergespann aufgelöst haben. Schwalb bereitet die Gründung eines eigenen Labors vor, Gressel hat ihre Doktorarbeit beendet und ist auf der Suche nach einer neuen Stelle. „Es ist immer so: Wenn die Leute die besten Sachen machen, dann muss man sie loslassen“, gibt Cramer zu und ist sichtlich stolz auf die beiden.
Letzte Änderungen: 10.10.2019