Western Blot mit
Southern Blot
(11.05.2022) Mit einem simplen Kontakt-Blotting-Verfahren kann man Proteine nach einer nativen Agarose-Gelelektrophorese auf eine Membran übertragen.
Um Western Blots von nativen Proteinen durchführen zu können, werden die Proteine meist in einem Polyacrylamid-Gel (PAGE) elektrophoretisch getrennt, das den Farbstoff Coomassie-Blau enthält. Das negativ geladene Coomassie-Blau bindet bei dieser Blue-native-PAGE an die Proteine und hüllt sie ähnlich wie Natriumlaurylsulfat oder besser bekannt als „sodium dodecycl sulfate“ (SDS) mit einer negativen Ladung ein – jedoch ohne ihre native Struktur zu zerstören. Bei einem anschließenden Western Blot, etwa mit einer Elektroblot-Apparatur, wandern die negativ geladenen Proteine alle im Gleichmarsch zur Anode.
Die Blue-native-PAGE ist aber oft eine ziemliche Schweinerei. Ein Protein-Analyse-Dienstleister aus den USA entwickelte daher ein Protokoll für die native Gelelektrophorese, bei dem man die Proteine in einem Agarose-Gel trennt (Int J Biol Macromol, 140:668-671). Als Laufpuffer verwendet das Team ein Histidin/2-(N-morpholino)ethansulfonsäure-System (His/MES) mit einem pH-Wert von 6,1. Je nach Ladung wandern die Proteine in diesem zur Anode oder zur Kathode. Der Kamm für die Probetaschen steckt daher in der Mitte des horizontalen Agarose-Gels.
5-Minuten-Transfer mit 3-kg-Block
Wie aber kann man die ungeladenen nativen Proteine aus dem Agarose-Gel auf eine Western-Blot-Membran übertragen? Die Antwort hierauf ist ein verblüffend einfaches Kontakt-Blotting-Verfahren, das an den guten alten Southern Blot erinnert.
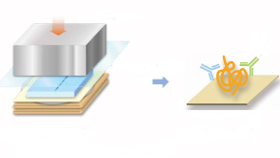
Für das Kontakt-Blotting benötigt man als untere Schicht zwei dicke Lagen trockenes Filterpapier. Auf dieses platziert man ein 0,19-Millimeter-Whatman-Papier und darauf die auf die Größe des Gels zurechtgeschnittene PVDF-Membran, die vorher mit Methanol oder Ethanol vorbehandelt wurde. Anschließend legt man das klatschnasse Agarose-Gel direkt nach der Gelelektrophorese auf die Membran und deckt es mit einer Frischhaltefolie ab. Jetzt muss man nur noch einen etwa drei Kilogramm schweren (Aluminium-)Block (für ein 6 x 6 Zentimeter Gel) auf das Ganze legen, um den nötigen Druck von 80 Gramm pro Quadratzentimeter für das Kontakt-Blotting aufzubauen. Der Transfer dauert ungefähr fünf Minuten, danach ist die noch feuchte Membran bereit für die üblichen Blockier- und Nachweis-Schritte.
Mechanismus unklar
Das Team nutzte die Technik für Western Blots von Proteinen mit unterschiedlichen isoelektrischen Punkten (pI 4,5 bis 10,7) und Größen (42 bis 150 kDa). Der genaue Mechanismus des Transfers ist der Gruppe nicht ganz klar, sie vermutet aber, dass Diffusion sowie hydrophobe Interaktionen die treibenden Kräfte sind. Für den Kontakt-Blot eignen sich sowohl PVDF-Membranen mit Porengrößen von 0,2 Mikrometern als auch 0,45 Mikrometern.
Ein wesentlicher Vorteil des Verfahrens besteht darin, dass man die geblotteten Proteine mit Konformations-spezifischen Antikörpern detektieren kann. Dem Team gelang es beispielsweise in Extrakten von HEK293-Zellen, die SARS-CoV-2-Spike-Proteine exprimierten, die Alpha- von der Delta-Variante zu unterscheiden.
Andrea Pitzschke
Sakuma C. et al. (2022): Western blotting of native proteins from agarose gels. Biotechniques, DOI: 10.2144/btn-2022-0012
Bild: Sakuma C. et al.