Neues Muskel-Modell
(15.4.16) Jenaer und Stuttgarter Forscher haben ein korrigiertes Modell der Muskelkontraktion entwickelt: Die sogenannten Z-Scheiben sind demnach keine feste Mauer, an die die Filamente anstoßen, sondern eher ein durchlässiger Netz-Vorhang.
Quergestreifte Muskelfibrillen bestehen aus vielen tausend Sarkomeren, in denen dünne Aktinfilamente in sogenannten I-Bändern angeordnet sind. An den Seitenenden der Sarkomere sind die I-Bänder an Zwischenscheiben (Z-Scheiben) verankert. Die Struktur dieser Z-Scheiben besteht unter anderem aus Aktinfilamenten benachbarter Sarkomere, die über α-Actinin vernetzt sind.
Bei der Muskelkontraktion wandern die Köpfchen der Myosinfilamente an den Aktinfilamenten entlang und ziehen unter ATP-Verbrauch daran. „Dadurch verkürzen sich die Fasern und die Filamente gleiten aneinander vorbei“, erläutert der Muskelexperte Christian Rode von der Friedrich-Schiller-Universität Jena. Troponin und Tropomyosin regulieren dabei die Bindung von Myosin an die Aktinfilamente.
Dem neuen Modell zufolge gleiten die Myosin-Filamente bei der Kontraktion gestreifter Muskulatur durch die netzartige Struktur der Z-Scheiben hindurch.
Bisher hatte man vermutet, dass sie dort zusammengestaucht werden. „Dafür sind die Myosinfilamente aber viel zu steif”, erläutert Erstautor Rode. „Biophysikalische Daten belegen, dass Muskeln nicht in der Lage sind, die nötige Kraft dafür zu erzeugen.“ Das Modell veröffentlichten die Jenaer und Stuttgarter Wissenschaftler kürzlich unter dem Titel „Myosin filament sliding through the Z-disc relates striated muscle fibre structure to function“ in den Proceedings of the Royal Society B(DOI: 10.1098/rspb.2015.3030).
Platz für das Hindurchgleiten
Das neue Modell, in das veröffentlichte sowie eigene Daten einflossen, ist besser mit experimentellen Beobachtungen vereinbar als die bisher etablierte Vorstellung über die Funktionsweise der Muskelkontraktion. Zum Beispiel mit Hinblick auf die isometrische Kraftentwicklung. „Isometrisch bedeutet: bei konstanter Länge des Muskels. Das muss man sich so vorstellen: Wenn wir einen Muskel an den Sehnen festhalten und elektrisch stimulieren, stellt sich nach einiger Zeit eine konstante Kraft ein, die isometrische Muskelkraft. Zu diesem Zeitpunkt ist die Sehne gedehnt und die Muskelfaser verändert ihre Länge nicht mehr“, erläutert Rode.
Im Überlappungsbereich der Filamente im Sarkomer haben die Aktinfilamente normalerweise eine hexagonale Anordnung. An den Z-Scheiben sind sie dagegen in einer tetragonalen Anordnung befestigt.
„Auf diese Weise ist nach unserem Modell Platz vorhanden für das Hindurchgleiten der Myosinfilamente durch die Z-Scheiben“, erklärt der Forscher. Rode vermutet, dass das Muskelprotein Titin die Ausrichtung der Myosinfilamente im tetragonalen Gitter der Aktinfilamente erleichtert. Man weiß, dass Titin die Myosinfilamente an den Z-Scheiben verankert und dort auch mit den Aktinfilamenten verbunden ist.
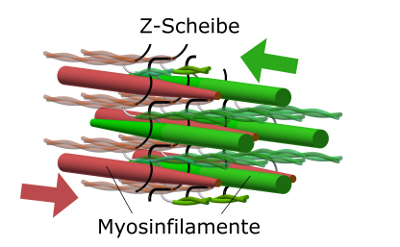
Ausschnitt der Mikrostruktur gestreifter Muskulatur: Die Myosinfilamente (rot und grün) zweier benachbarter Sarkomere durchdringen die maschenartige Struktur der Z-Scheibe. Quelle: Christian Rode/FSU Jena
Stoßdämpfer
Nach dem Passieren der Z-Scheibe richten sich im benachbarten Sarkomer die Brücken zwischen Myosin- und Aktinfilamenten gemäß der Polarität der Aktinfilamente aus, so das Modell. Die entwickelte isometrische Kraft entspricht dabei dem Ausmaß der Überlappung zwischen Aktin und Myosin. Sind die erzeugten Kräfte gegenläufig, schwächen sie sich gegenseitig ab und reduzieren die Kontraktionsgeschwindigkeit der Faser.
„Das könnte der physiologische Grund für das Vorhandensein eines zweiten Myosinkopfes sein. So kann jedes Myosinmolekül an Aktinfilamente unterschiedlicher Polarität binden. Die beobachtete Abnahme der Kontraktionsgeschwindigkeit bei bereits kurzen Sarkomeren könnte eine Art Stoßdämpfermechanismus zum Schutz des Muskels sein“, führt Rode aus. Dysfunktionale Z-Scheiben könnten nach Ansicht der Forscher bei der Duchenne-Muskeldystrophie und beim Sjögren-Syndrom zur Muskelschwäche beitragen.
Muskelforscher mit Kenntnissen in Mathematik und Sport
Dass der Anhang der Veröffentlichung voller mathematischer Formeln steckt, ist kein Zufall. Rode, der als Postdoc am Lehrstuhl für Bewegungswissenschaft bei Reinhard Blickhan an der Friedrich-Schiller-Universität in Jena arbeitet, hat dort auch ein Studium in Mathematik und Sport auf Lehramt an Gymnasien abgeschlossen. Bereits für seine Staatsexamensprüfung hat er Muskelmodelle erstellt und den Einfluss der Sehne auf die Leistungserzeugung im Muskel untersucht. Danach hat er bei Blickhan zum Thema der Interaktion zwischen passiven und kontraktilen Muskelelementen promoviert.
„Bis Herbst 2015 war ich auch mit der TU Darmstadt assoziiert. Dort habe ich im Rahmen des EU-Projekts Balance an der Entwicklung eines Laufroboters mitgearbeitet, der von außen wie ein Exoskelett anschnallbar ist. Dieser soll Menschen helfen, beim Gehen und Stehen die Balance zu halten“, berichtet der Forscher. „Für die Veröffentlichung in den Proceedings of the Royal Society B habe ich mit Tobias Siebert vom Institut für Sport- und Bewegungswissenschaft der Universität Stuttgart zusammengearbeitet, mit dem ich insgesamt acht gemeinsame Publikationen habe. Wir kennen uns aus seiner Zeit an der Universität Jena. Er hat Erfahrung mit Muskelexperimenten, während ich eher theoretisch arbeite und modelliere“, so Rode. „Zusammen mit AndréTomalka konnte Siebert zeigen, dass die Krafterzeugung bei bereits stark verkürzten Sarkomeren nicht nur bei Fröschen zu beobachten ist, sondern auch bei Ratten. Mein Chef, Reinhard Blickhan, hat die Abschätzungen der Myosinsteifigkeit beigetragen.“
Bisher berücksichtige das Modell allerdings nicht, dass sich die seitlichen Abstände der Filamente bei der Verkürzung ändern, bemerkt der Postdoc.
Obwohl Rode bisher an dreizehn Veröffentlichungen mitgewirkt hat und weitere noch im Begutachtungsprozess sind, ist seine wissenschaftliche Zukunft noch ungewiss, wie bei so vielen Nachwuchsforschern. Für die Erweiterung des Muskelmodells sollen Gelder beantragt werden. „Leider wird der Lehrstuhl von Blickhan im Zuge seiner Emeritierung aus Haushaltsgründen abgebaut. Dadurch verliere ich meine Stelle und weiß noch nicht, ob ich meine Habilitation auch abschließen kann.“ Der Nachwuchsforscher hofft auf erfolgreiche Anträge und sich eröffnende Chancen.
Bettina Dupont
Letzte Änderungen: 02.06.2016









