Nachhaltige Zellfabriken
(13.8.15) Pharmafirmen, Waschmittelhersteller oder die chemische Industrie: Sie alle benötigen Enzyme in rauen Mengen. Der weltweite Markt ist ca. 5,1 Milliarden Euro pro Jahr wert. Können Zellfabriken auf Cyanobakterien-Basis in diesem Geschäft mitspielen?
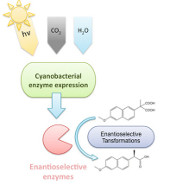
Zellfabriken mit Photosynthese-treibenden Bakterien wären ein Traum an Nachhaltigkeit für die großindustrielle Herstellung von Enzymen. Die Idee: Licht, Wasser, Kohlendioxid und ein paar Salze sollten reichen, denn die eigentliche Syntheseleistung erledigen zellfreie Cyano-Kulturen mit Energie aus der Fotosynthese. Anders als heterotrophe bakterielle Zellfabriken müsste man Cyanobakterien-Kulturen also nicht zufüttern, z.B mit Rübenzucker aus der Agrarwirtschaft.
Wenn für diesen Schritt der Enzymproduktion kein Bauer mit dem Traktor übers Feld fahren müsste, würde das Ressourcen sparen und die Erdöl-Vorräte schonen.
Das Problem ist allerdings, dass man die Cyanobakterien entsprechend modifizieren muss, damit sie die gewünschten Enzyme in lohnender Menge herstellen; und zwar möglichst ohne störende Nebenprodukte. Zudem müssen die Biotechnologen die Tücken der Stereochemie unter Kontrolle bringen, damit möglichst nur jeweils das gewünschte Enantiomer (eine von zwei spiegelbildlichen Ausführungen der Enzyme) entsteht.
Dass Cyanos für die Enzym-Großproduktion im Prinzip gut geeignet sind, zeigt jetzt eine Machbarkeitsstudie von Forschern um Marc Nowaczyk und Robert Kourist von der Ruhr-Universität Bochum (Microbial Cell Factories 14:53). Die Bochumer stellten beispielsweise eine Esterase aus dem thermophilen Bakterium Sulfolobus tokodai in einer Kultur des Cyanobakteriums Synechocystis her. Auch eine Arylmalonat-Decarboxylase aus Bordetella bronchiseptica konnten die Cyanos produzieren – in beiden Fällen in recht ordentlicher Ausbeute und mit ausgezeichneter Enantiomer-Selektivität.
Im direkten Vergleich zu einem etablierten Echerichia coli-System erreichte die phototrophe Expression in dieser Machbarkeitsstudie allerding nur eine Ausbeute von 25 Prozent – aber eben wie gesagt ohne den zusätzlichen Aufwand für die Herstellung von Bakterienfutter.
„Besonders wichtig war die Beobachtung, dass die Zellbestandteile der Cyanobakterien mit der katalytischen Aktivität kompatibel sind“, fasst Letztautor Robert Kourist zusammen. Kourist ist überzeugt: "Die Fotosynthese zu nutzen, um industrielle Enzyme aus Kohlendioxid und Wasser herzustellen, ist ein neuer und umweltfreundlicher Ansatz.“
Um die „grünen Zellfabriken“ erfolgreich im großen Maßstab anwenden zu können, muss die Technologie allerdings noch effizienter werden.
Hans Zauner
Grafik: Abb. 1 aus Bartsch et al., Microbial Cell Factories 14:53, CC-BY
Quellen:
- Microbial Cell Factories 14:53
- Pressemitteilung der Ruhr-Universität Bochum
Letzte Änderungen: 25.09.2015